Sección 1
Observa estos vídeos y contesta las preguntas propuestas:
1. La química del fósforo
2. La química de losfuegos pirotécnicos
4. Reacción endotérmica
1. ¿Cuáles son las
sustancias químicas que se utilizan para los fósforos?
2. ¿Qué sustancias
conforman la banda lateral de la caja de
fósforos?
3. ¿Qué función cumple
durante la reacción cada uno de los componentes del fósforo?
4. ¿Qué función
cumplen las sustancias de la banda lateral de la caja de fósforos?
5. ¿Por qué se
necesita fricción para encender un fosforo?
6. ¿La cabeza de los
cerillos puede reaccionar en el vacío si la temperatura es lo suficientemente
alta?
7. ¿Por qué el agua
que se agrega sobre la madera se congela al
colocar sobre ella el recipiente donde ocurre la reacción entre el
hidróxido bario y el cloruro de amonio?
8. ¿En cuál de las
reacciones mostradas se adsorbe energía y
en cuál se libera energía?
9. ¿El fósforo para
encender inicialmente necesita del oxígeno?
Finalmente construye un párrafo con tus propias palabras indicando cómo funciona un fósforo
Sección 2
EN el laboratorio de química
Preguntas de indagación
Preguntas de indagación
1. ¿Qué entendemos por
reacción viable? ¿Qué determina que una reacción transcurra de manera natural?
2. Busca la definición de estos conceptos:
entropía, entalpía, energía libre de Gibbs y cómo se relacionan estos para
determinar que un proceso sea viable o no lo sea.
4. ¿Cómo varió la
entalpía y la entropía en cada una de las reacciones realizadas en laboratorio?
5. ¿Qué reacciones
conoces que liberen energía a los alrededores?
¿Qué reacciones conoces que
absorban energía de los alrededores?
6. ¿Qué cambio de
entalpía tienen las reacciones endotérmicas y exotérmicas?
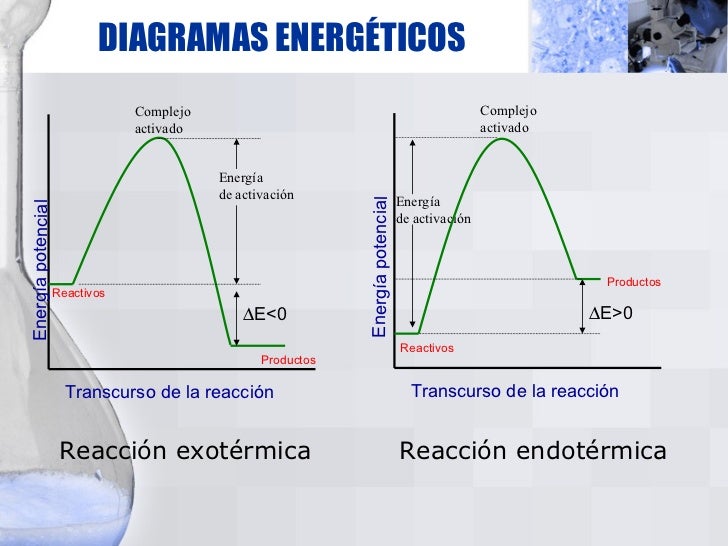
7. Observa los siguientes diagramas de energía
potencial (diagramas de energía)
(figura 3) Figura 3. Representación del transcurso de una reacción exotérmica y
endotérmica. Imagen tomada de http://image.slidesharecdn.com/reaccionesqumicas-100319045149-phpapp01/95/reacciones-qumicas-25-728.jpg?cb=1268974371
7. Según la variación
de energía representada en los diagramas ¿Por qué algunas reacciones liberan
energía y otras la adsorben?
8. ¿Todas las reacciones
que liberan energía ocurrirán de manera natural, sin interferencia del hombre?
9. ¿Cómo es la
variación de entropía y entalpía en procesos espontáneos y no espontáneos?
10. ¿Por qué el hielo
al fundirse adsorbe energía mediante una trasferencia en forma de calor?
11. ¿En qué estado las
moléculas de agua, en promedio, tienen más energía potencial?
Sección 3
Fotocopias guía trabajo
Sección 4
Lectura Metabolismo y energía (guía de trabajo)